Заведующая лабораторией:

Агекян Ася Агековна, кандидат химических наук (к.х.н.)
ORСID: ID 0000-0001-6151-4951
Телефон: (+37410) 285-101
E-mail: aaghekyan@mail.ru
Основное направление исследований
Синтез новых кислород- и азотсодержащих гетероциклических соединений, регулирующих деятельность сердечно-сосудистой и центральной нервной систем, а также обладающих антимикробной, антигипоксической, антимоноаминоксидазной, противосудорожной и антиоксидантной активностью среди производных 1,3-бензодиоксола, 1,4-бензодиоксана, пятичленных гетроциклов с двумя или тремя гетероатомами, 4-спирозамещенного тетрагидроизохинолина и его нециклизованных аналогов.
История лаборатории
Основана и возглавлена в 1955 году кандидатом химических наук Африкян Вардуи Георгиевной. Лаборатория занималась синтезом новых ароматических и гетероциклических аминоэфиров, влияющих на сердечно-сосудистую систему, и изучением их биологических свойств, с целью выявления связи между химической структурой и биологической активностью. В результате исследований был открыт ряд лекарственных препаратов: Фубромеган, Кватерон и Ганглерон, которые нашли широкое применение в медицинской практике.
В 1970 году лабораторию возглавил доктор химических наук, профессор Маркарян Эдуард Абресович, который, расширив рамки, начал исследования в области синтеза диарилпропионовых кислот, арилалкиламинов, конденсированных гетероциклических систем: индола, изохинолина, бензазепина, бензодиоксана, изохромана. В результате был выявлен ряд потенциальных лекарственных препаратов: Фобуфол, Дифалкин, Эмакор, Бедитин, Меседин.
С 2011 года лабораторию возглавляет кандидат химических наук Агекян Ася Агековна, которая продолжила основное направление исследований – целенаправленный синтез биологически активных соединений в ряду азот- и кислородсодержащих гетероциклических аннелированных систем. Результаты работ представлены в многочисленных научных публикациях.
Текущая деятельность
В лаборатории работают 8 высококвалифицированных специалистов, в том числе 4 кандидата наук
Лучшие результаты
✔ Разработаны оптимальные условия для синтеза 4-спироциклоалканзамещенных производных тетрагидроизохинолина, содержащих во втором положении амино- и сульфаниламидные, алканольные и гетерилалкильные фармакофорные фрагменты
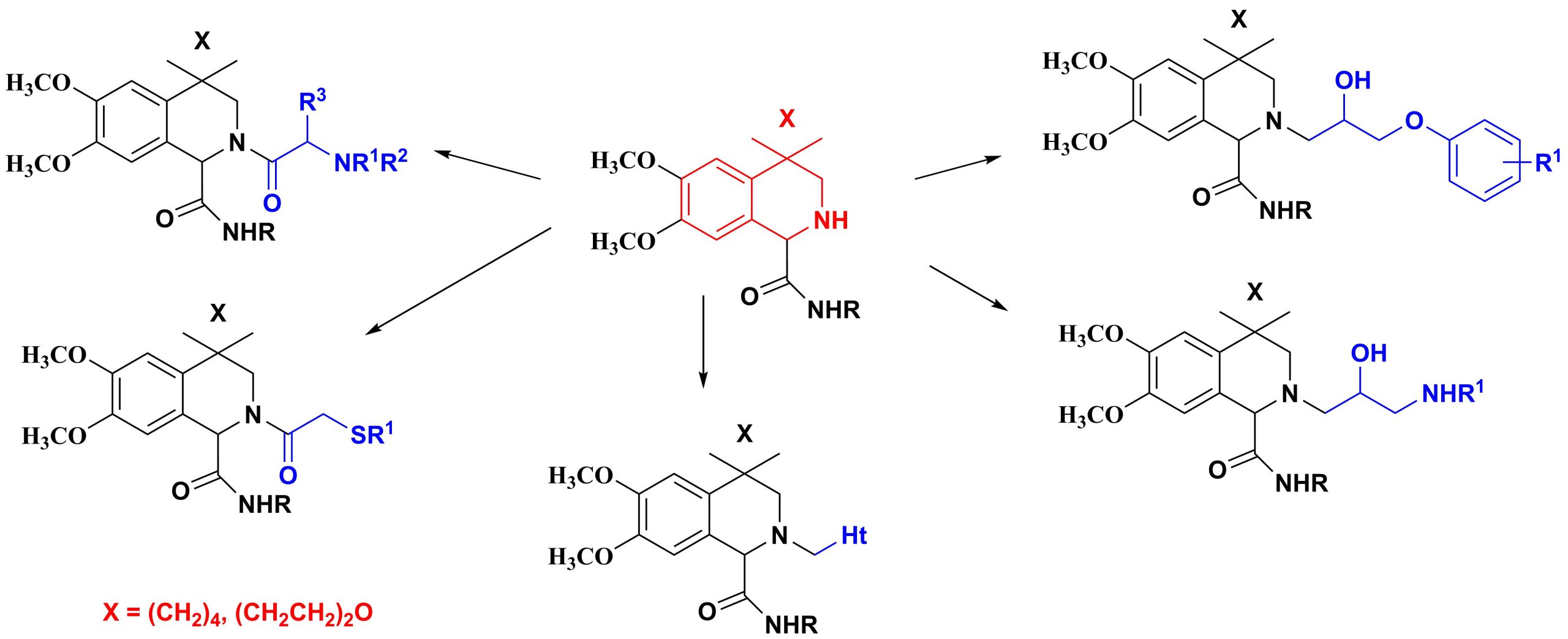
Russ. J. Org. Chem., 2013, v. 49, No. 11, pp. 1632-1636. doi: 10.1134/S1070428013110122
Russ. J. Org. Chem., 2016, v. 52, No. 5, pp. 689-693. doi:10.1134/S1070428016050122
Russ. J. Org. Chem., 2022, v. 58, No. 11, pp. 1581-1588. doi:10.1134/S1070428022110045
Russ. J. Org. Chem., 2019, v. 55, No. 3, pp. 302-307. doi:10.1134/S1070428019030047
Russ. J. Org. Chem., 2015, v. 51, No. 2, pp. 221-225. doi:10.1134/S1070428015020153
✔ Предложен новый подход к синтезу производных тетрагидроизохинолина, содержащих две метильные группы в 4-м положении, на основе замещенных бензиламинов.
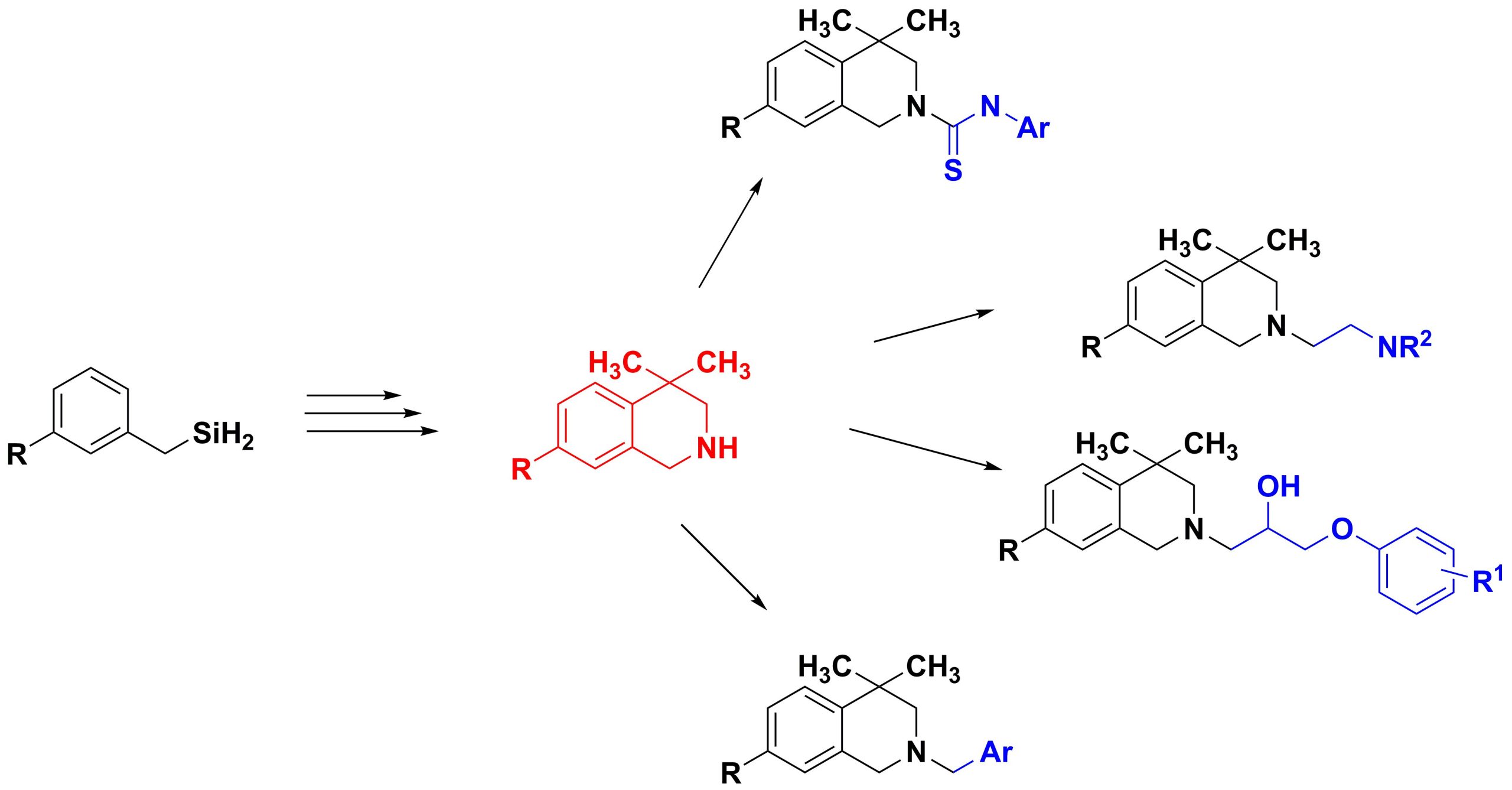
Russ. J. Org. Chem., 2017, v. 53, No. 3, pp. 362-365. doi:10.1134/S1070428017030083
Russ. J. Org. Chem., 2022, v. 58, No. 10, pp. 1409-1415. doi:10.1134/S1070428022100049
✔ Разработаны методы синтеза различных производных 1,4-бензодиоксана, содержащих во втором положении замещенное 1,2,4-триазольное кольцо
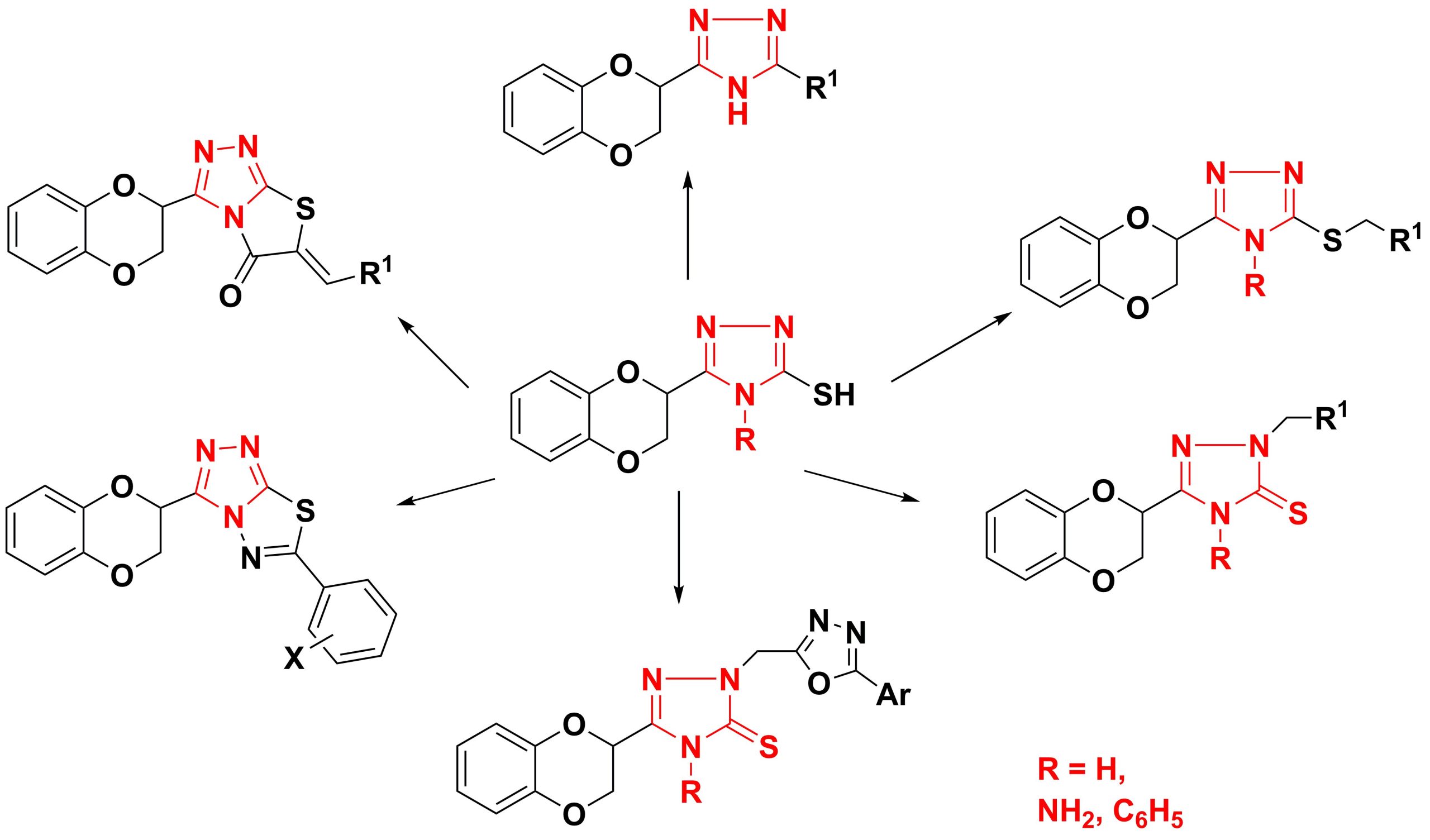
Russ. J. Org. Chem., 2017, v. 53, No. 3, pp. 428-432. doi:10.1134/S1070428017030198
Russ. J. Gen. Chem., 2018, v. 88, No. 4, pp. 839-842. doi:10.1134/S1070363218040345
Russ. J. Org. Chem., 2020, v. 56, No. 3, pp. 436-439. doi:10.1134/S1070428020030112
Chem. J. Armenia, 2023, v. 76 № 1-2, pp. 104-108
Russ. J. Org. Chem., 2021, v. 57, No. 7, pp. 1068-1072. doi:10.1134/S107042802107006X
✔ Осуществлен синтез и изучены некоторые превращения производных 1,4-бензодиоксана, содержащих во втором
положении гетероциклические кольца 1,3,4-оксадиазола и 1,3,4-тиадиазола.
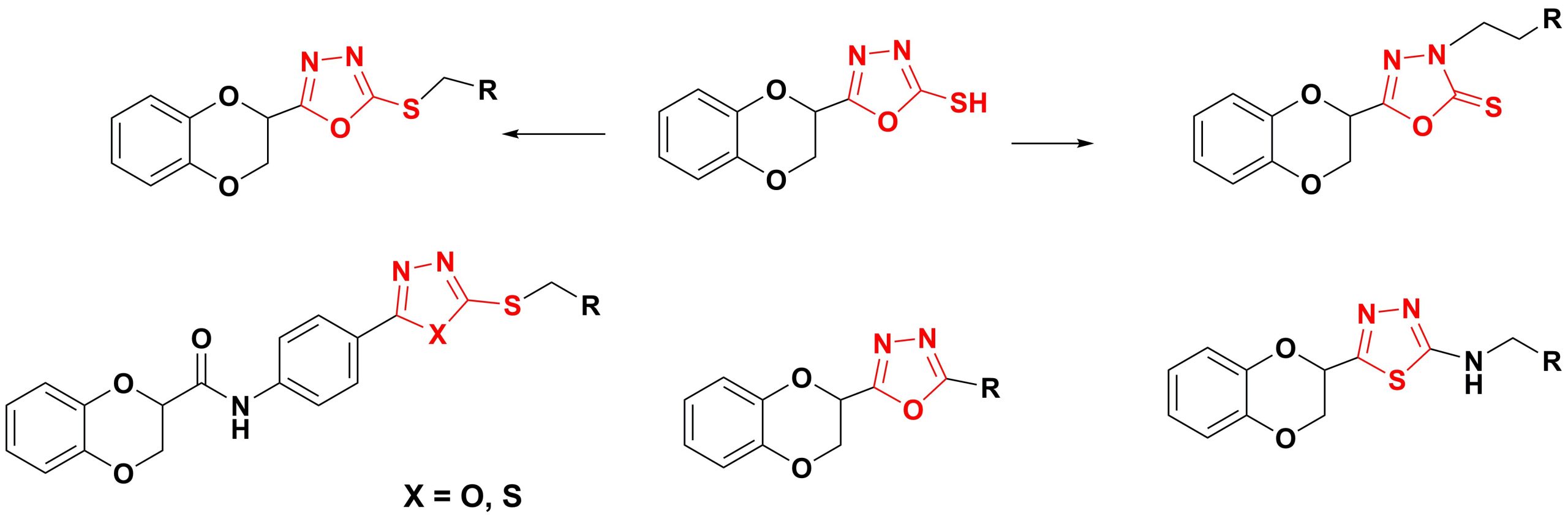
Russ. J. Org. Chem., 2020, v. 56, No. 3, pp. 385-389. doi:10.1134/S1070428020030033
Russ. J. Org. Chem., 2014, v. 50, No. 3, pp. 434-438. doi:10.1134/S1070428014030233
Russ. J. Org. Chem., 2024, v. 60, No. 9, pp. 1685-1691. doi:10.1134/S1070428024090100
Russ. J. Org. Chem., 2017, v. 53, No. 12, pp. 1905-1908. doi:10.1134/S1070428017120259
✔ Разработаны пути синтеза диамидных производных п-аминобензойной кислоты, содержащих фрагменты арилциклоалкана и 1,4-бензодиоксана.
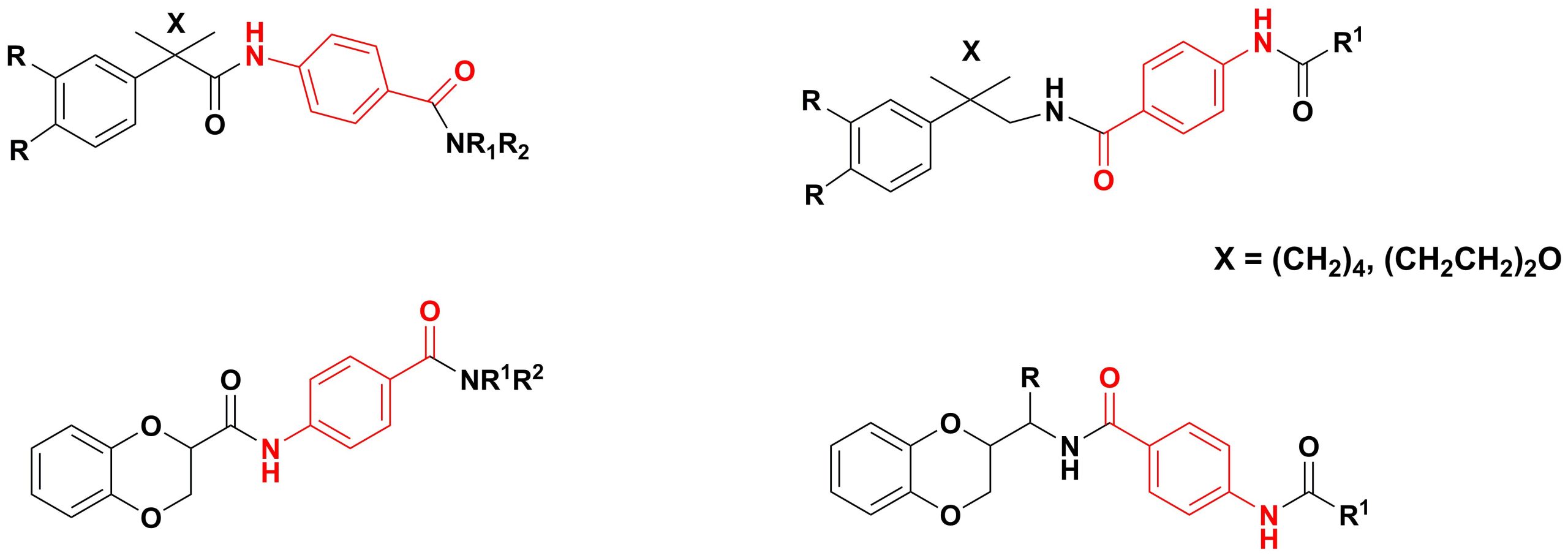
Russ. J. Gen. Chem., 2015, v. 85, No. 5, pp. 1057-1062. doi:10.1134/S1070363215050096
Chem. J. Armenia, 2012, v. 65, № 2, pp. 230-238
Chem. J. Armenia, 2016, v. 69, № 1-2, pp. 111-120
Russ. J. Org. Chem., 2012, v. 48, No. 7, pp. 972-976. doi:10.1134/S1070428012070147
✔ Разработаны пути синтеза новых арилоксипропаноламинов на основе арилциклопентан(тетрагидропиран, диметил)метиламинов
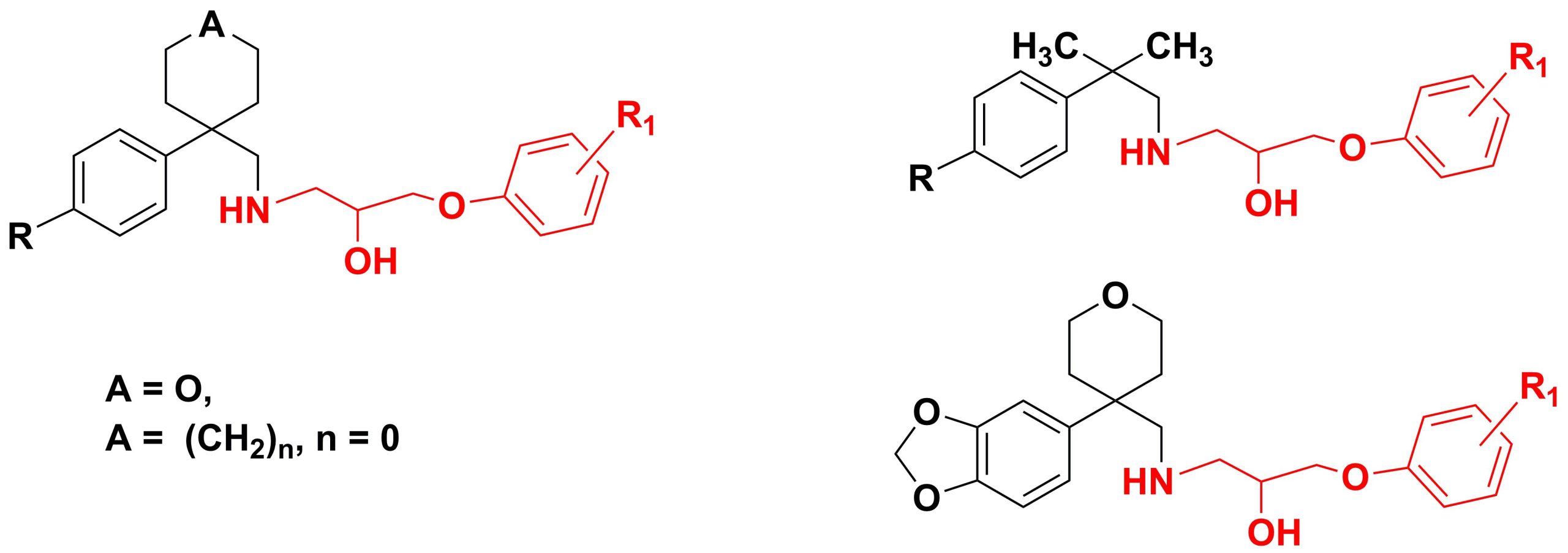
Russ. J. Org. Chem., 2016, v. 52, No. 2, pp. 209-213. doi:10.1134/S1070428016020081
Russ. J. Org. Chem., 2023, v. 59, No. 5, pp. 756-763. doi:10.1134/S1070428023050020
Russ. J. Org. Chem., 2024, v. 60, No. 1, pp. 18-24. doi:10.1134/S1070428024010032
✔ Разработаны пути синтеза разнообразных диамидных производных двухосновных карбоновых кислот (щавелевой, янтарной и малеиновой)
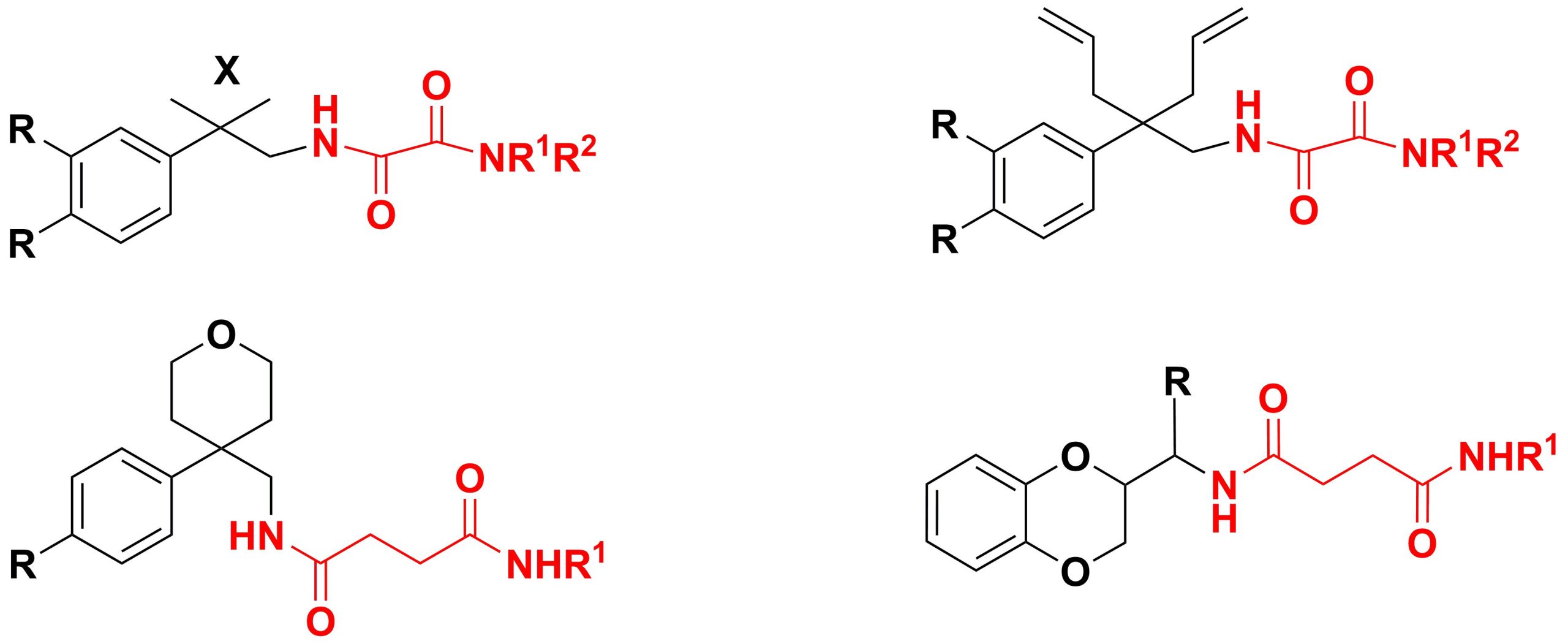
Russ. J. Org. Chem., 2013, v. 49, No. 7, pp. 1083-1086. doi:10.1134/S1070428013070221
Chem. J. Armenia, 2012, v. 65, № 2, pp. 215-223
Chem. J. Armenia, 2012, v. 65, № 3, pp. 332-341
Chem. J. Armenia, 2013, v. 66, № 4, pp. 628-635
Chem. J. Armenia, 2012, v. 65, № 1, pp. 111-117
Russ. J. Org. Chem., 2018, v. 54, No. 6, pp. 886-891. doi:10.1134/S1070428018060106
Russ. J. Org. Chem., 2024, v. 60, No. 11, pp. 2117-2124. doi:10.1134/S1070428024110046
✔ Впервые разработаны методы синтеза новых аминоамидов и аминоэфиров – производных арил-, 1,3-бензодиоксол-5-ил- и 1,4-бензодиоксан-6-илциклоалкан(тетрагидропиран)карбоновых кислот.
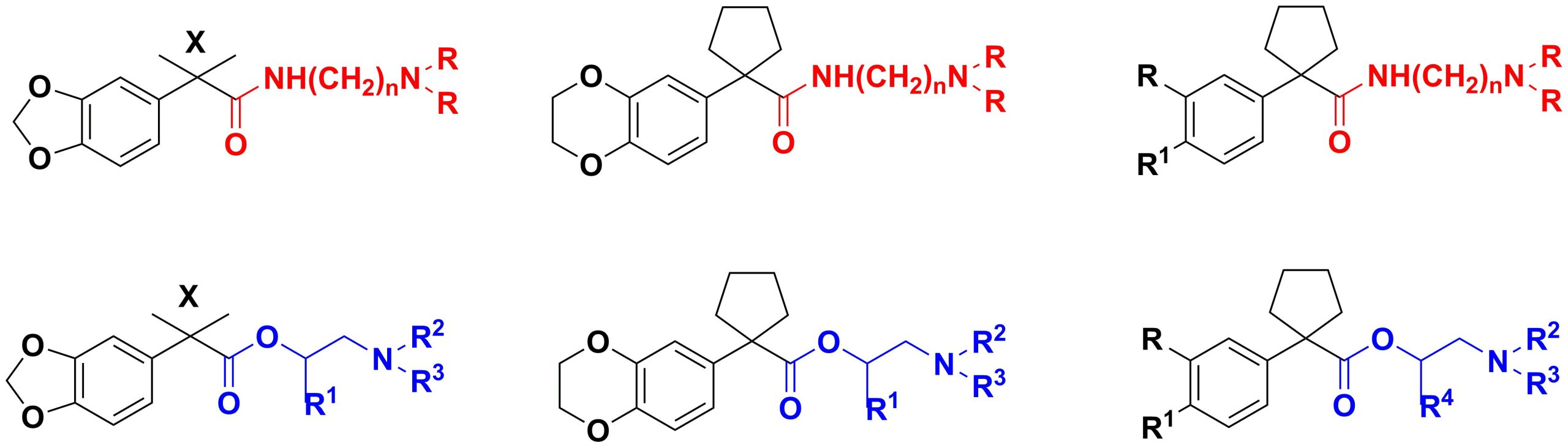
Russ. J. Gen. Chem., 2019, v. 89, No. 5, pp. 1051-1054. doi:10.1134/S107036321905027X
Russ. J. Org. Chem., 2024, v. 60, No. 6, pp. 1028-1035. doi:10.1134/S1070428024060071
Russ. J. Org. Chem., 2019, v. 55, No. 6, pp. 796-799. doi:10.1134/S1070428019060095
Russ. J. Org. Chem., 2025, v. 61, No. 3, pp. 403-411. doi:10.1134/S107042802560010X
✔ Разработаны методы получения производных 1,3,4-оксадиазола с кислородсодержащими гетероциклами (1,4-бензодиоксан, тетрагидропиран, фуран) во втором положении кольца.
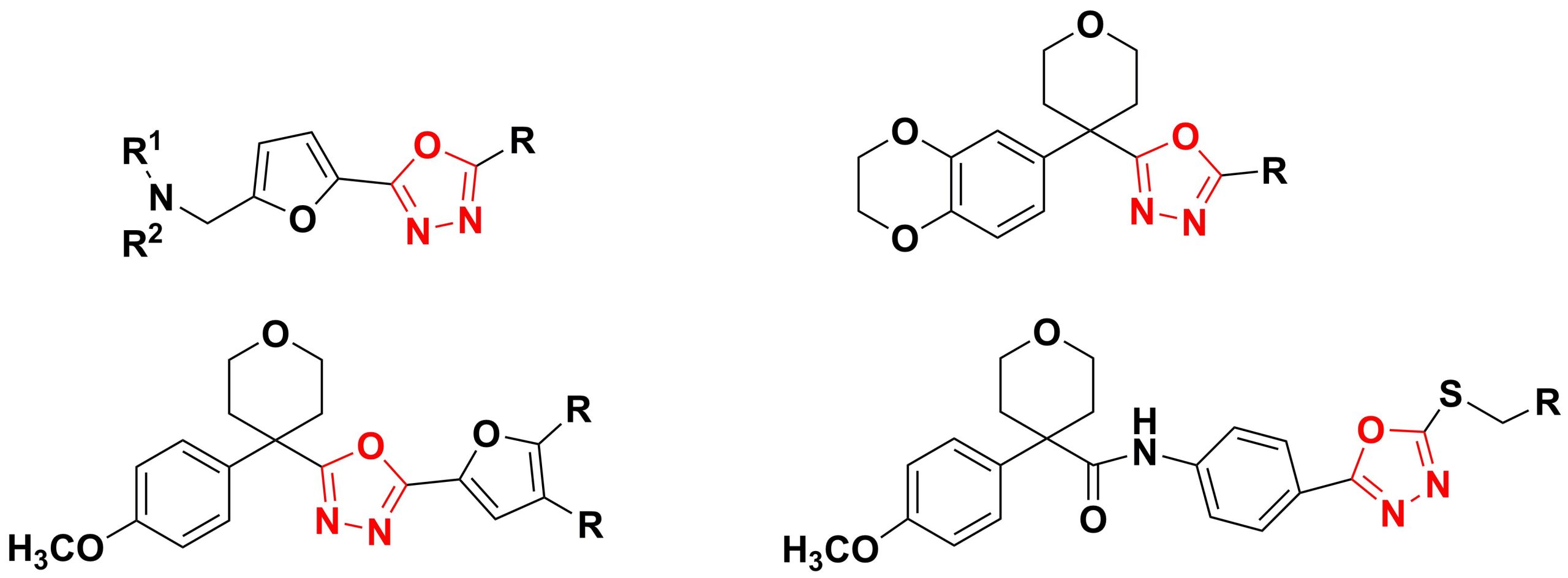
Russ. J. Org. Chem., 2025, v. 61, No. 1, pp. 73-79. doi:10.1134/S1070428024602966
Russ. J. Org. Chem., 2024, v. 60, No. 4, pp. 655-663. doi:10.1134/S1070428024040146
Russ. J. Org. Chem., 2020, v. 56, No. 2, pp. 281-286. doi:10.1134/S1070428020020177
✔ Предложены методы синтеза тиенопиримидинов, содержащих фрагменты 1,4-бензодиоксана и
фенилциклогексанкарбонитрила, циклизацией 2-амино-3-карбэтоксизамещенных тиофенов.
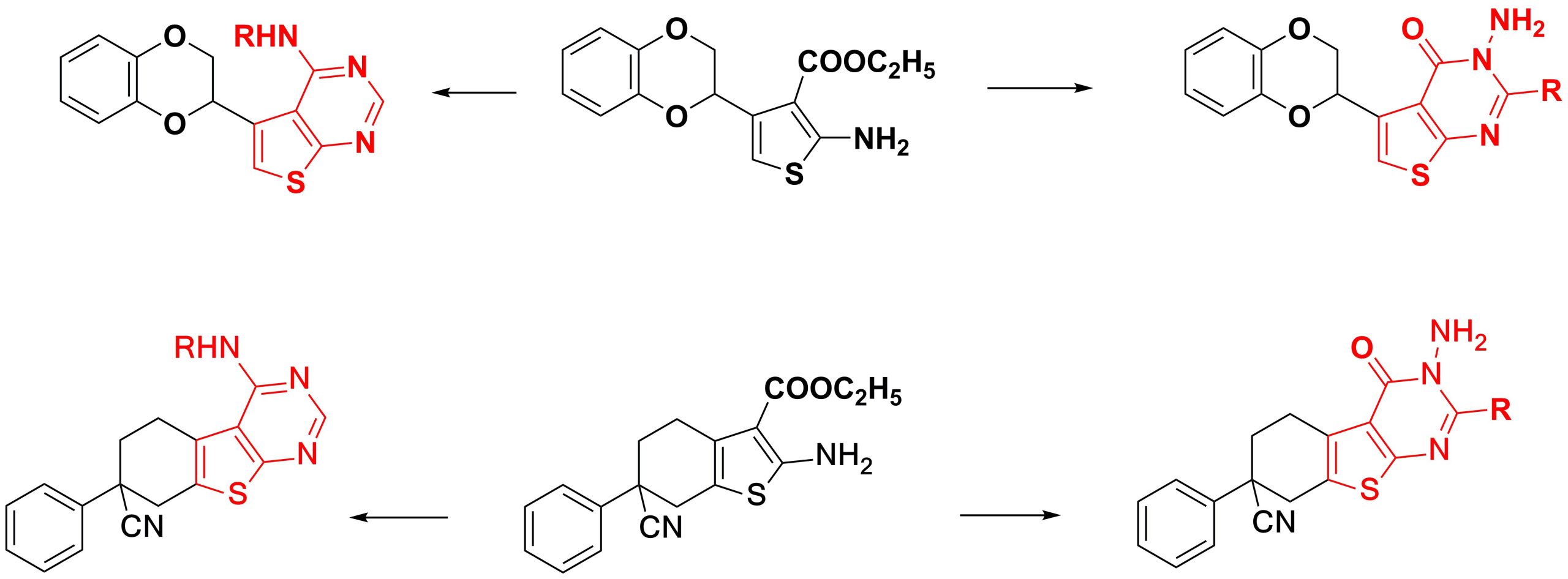
Russ. J. Org. Chem., 2019, v. 55, No. 5, pp. 598-601. doi:10.1134/S1070428019050038
Russ. J. Org. Chem., 2022, v. 58, No. 7, pp. 977-981. doi:10.1134/S1070428022070053
Russ. J. Org. Chem., 2024, v. 60, No. 3, pp. 397-402. doi:10.1134/S1070428024030047
Russ. J. Org. Chem., 2020, v. 56, No. 3, pp. 440-445. doi:10.1134/S1070428020030124
Russ. J. Org. Chem., 2021, v. 57, No. 10, pp. 1638-1642. doi:10.1134/S1070428021100110
✔ Исследованы антигипоксические, антимоноаминоксидазные, антиоксидантные, антиаритмические, противосудорожные и антибактериальные свойства синтезированных соединений
Лучшие работы последних лет
Russ. J. Org. Chem., 2021, v. 57, No. 2, pp. 195-202. doi:10.1134/S1070428021020093
Russ. J. Org. Chem., 2021, v. 57, No. 7, pp. 1068-1072. doi:10.1134/S107042802107006X
Russ. J. Org. Chem., 2021, v. 57, No. 10, pp. 1638-1642. doi:10.1134/S1070428021100110
Russ. J. Org. Chem., 2022, v. 58, No. 7, pp. 977-981. doi:10.1134/S1070428022070053
Russ. J. Org. Chem., 2022, v. 58, No. 10, pp. 1409-1415. doi:10.1134/S1070428022100049
Russ. J. Org. Chem., 2022, v. 58, No. 11, pp. 1581-1588. doi:10.1134/S1070428022110045
Russ. J. Org. Chem., 2023, v. 59, No. 11, pp. 1884-1891. doi:10.1134/S1070428023110064
Russ. J. Org. Chem., 2024, v. 60, No. 1, pp. 18-24. doi:10.1134/S1070428024010032
Russ. J. Org. Chem., 2024, v. 60, No. 3, pp. 397-402. doi:10.1134/S1070428024030047
Russ. J. Org. Chem., 2024, v. 60, No. 9, pp. 1685-1691. doi:10.1134/S1070428024090100
Russ. J. Org. Chem., 2024, v. 60, No. 4, pp. 655-663. doi:10.1134/S1070428024040146
Russ. J. Org. Chem., 2024, v. 60, No. 11, pp. 2117-2124. doi:10.1134/S1070428024110046
Russ. J. Org. Chem., 2025, v. 61, No. 1, pp. 73-79. doi:10.1134/S1070428024602966
Russ. J. Org. Chem., 2025, v. 61, No. 3, pp. 403-411. doi:10.1134/S107042802560010X